元素周期表中的相对原子质量(也称原子量)是元素所有天然同位素质量的加权平均值,反映了该元素在自然界中各种同位素的丰度及其质量。以下是关键点的详细解释:
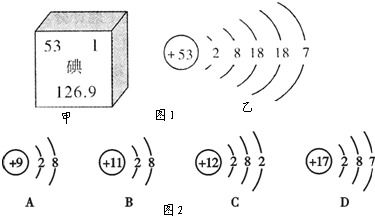
1. 定义与计算
相对原子质量(Atomic Weight)以碳-12同位素(¹²C)为基准,定义为:
[
ext{相对原子质量} = frac{
ext{元素的一个原子平均质量}}{frac{1}{12}
imes
ext{¹²C原子的质量}}
]
计算方法:
将每种天然同位素的质量数乘以其丰度(百分比),再求和。例如:
氯(Cl)有两种主要同位素:
[
ext{Cl-35(丰度75%)} quad
ext{和} quad
ext{Cl-37(丰度25%)}
]
[
ext{原子量} = (35
imes 0.75) + (37
imes 0.25) = 35.45
]
2. 为何不是整数?
大多数元素由多个同位素组成,原子量是它们的加权平均值,因此通常为小数。例如:
碳(C)的原子量为12.01(含¹²C、¹³C和微量¹⁴C)。
铜(Cu)的原子量63.55(约69% Cu-63和31% Cu-65)。
3. 特殊情况的标注
某些元素的同位素丰度因来源不同而变化,原子量会标注为区间值。例如:
氢(H):[1.00784, 1.00811](取决于水源中的氘含量)。
锂(Li):[6.938, 6.997](因矿物来源不同)。
4. 与质量数的区别
质量数(Mass Number):单个原子中质子与中子数之和(如¹²C的质量数为12)。
相对原子质量:所有同位素的平均值,可能包含小数。
5. 周期表中的标注
在标准周期表中,相对原子质量通常位于元素方格的下方,例如:
氧(O):16.00
铁(Fe):55.85
注意:某些版本可能四舍五入为整数,但科学计算需使用精确值。
6. 应用场景
化学计算:用于计算摩尔质量、反应计量等。
科研与工业:同位素分析、地质年代测定(如-238衰变)、核技术等。
7. 国际更新
国际纯粹与应用化学联合会(IUPAC)定期修订原子量数据。例如:
2013年,修改了12种元素(如铝、金)的原子量范围。
2021年,更新了铟(In)等元素的原子量。
总结:相对原子质量是元素在自然界中的“平均身份”,既体现了同位素多样性,也是化学与物理研究的基础数据。对于精确实验,需参考最新IUPAC数据或具体同位素组成。


